هل يجوز لعب دور الله؟
دكتور. يعمل Andrea Bannert مع منذ عام 2013. أجرى دكتور محرر الأحياء والطب في البداية بحثًا في علم الأحياء الدقيقة وهو خبير الفريق في الأشياء الصغيرة: البكتيريا والفيروسات والجزيئات والجينات. تعمل أيضًا كصحفية مستقلة في Bayerischer Rundfunk والعديد من المجلات العلمية وتكتب الروايات الخيالية وقصص الأطفال.
المزيد عن خبراء يتم فحص جميع محتويات بواسطة الصحفيين الطبيين.لأول مرة أصبح من الممكن إصلاح تغيير جيني في الأجنة البشرية بنجاح. ولكن ليس فقط الأمراض يمكن علاجها بالتكنولوجيا. يمكن أيضًا تحديد لون العين والميزات الأخرى مسبقًا بهذه الطريقة. هل سيكون الطفل المصمم قريبًا؟
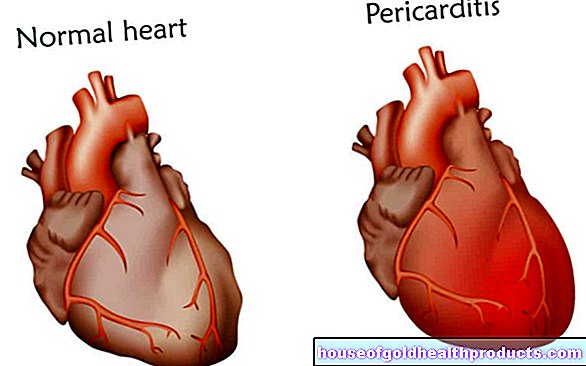
انهار Simon K. * أثناء التمرين ولم يستيقظ مرة أخرى. التشخيص: الموت القلبي المفاجئ. عانى الشاب الرياضي مما يُعرف باسم اعتلال عضلة القلب الضخامي أو HCM باختصار. في هذا المرض ، يثخن نسيج عضلة القلب في البطين الأيسر. هذا الاضطراب شائع نسبيًا. يصاب واحد من كل 500 شخص ويموت الكثيرون بسببه.
مقص يسعى للقادة
الشيء المميز في HCM: المعلومات ، ما يسمى بالشفرة الجينية ، تتغير فقط عند نقطة واحدة في جين محدد للغاية. يسمي العلماء هذا بالطفرة. هناك حوالي 10000 مرض وراثي آخر تنجم عن طفرات معزولة بالمثل. التليف الكيسي أو فقر الدم المنجلي - وهما مرضان يهددان الحياة بشكل متساوٍ. الفكرة الواضحة هي تصحيح الأخطاء الجينية الخطيرة في أقرب وقت ممكن.
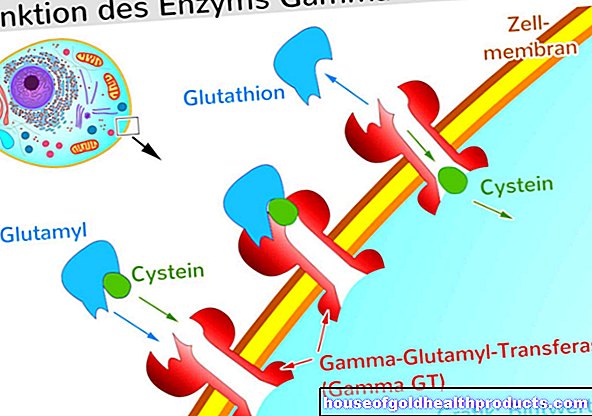
محاولة مستحيلة حتى وقت قريب. يعرف العلماء أنزيمات يمكنها "قطع" الحمض النووي ، لكن جزيئات البروتين هذه لا تتحدث نفس لغة المعلومات الجينية. هذا هو السبب في أنهم لا يستطيعون تعقب الخلل في الجينوم.
تغير ذلك مع اكتشاف مذهل للعالمين جينيفر دودنا وإيمانويل شاربنتير قبل أربع سنوات. بالصدفة وجدوا إنزيمًا في البكتيريا يمكنه قطع خيوط الحمض النووي وحمل مقتطف صغير من المادة الجينية معها مثل المترجم الفوري. يمكنه قراءة الكمية الهائلة من البيانات في الحمض النووي ويوجه المقص الجزيئي بالضبط حيث من المفترض أن يقطع. أطلق العلماء على الفريق الفعال اسم "CRISPR / Cas9" - تحتاج البكتيريا إليه للدفاع عن نفسها ضد الفيروسات.
مرض وراثي مقض في مهده
استخدمت مجموعة من الباحثين من جامعة أوريغون للصحة والعلوم في بورتلاند المقص الجيني لمحو اعتلال عضلة القلب الضخامي مبكرًا جدًا في الشفرة الوراثية - في الأجنة. قام فريق شوخرت ميتاليبوف بتجهيز المقص الجيني بتسلسل جيني يتعرف على الموقع الدقيق في الحمض النووي الذي يتم فيه برمجة المرض.
قاموا بتطبيق أداتهم الفائقة الجديدة على 58 جنينًا ، تم إنشاؤها من الحيوانات المنوية لرجل يعاني من HCM وخلايا بويضة امرأة سليمة. مثل هذه المحاولات ممكنة في الولايات المتحدة. ومع ذلك ، يمنع قانون حماية الأجنة في ألمانيا استخدام الأجنة البشرية لأغراض البحث.
معدل نجاح مذهل
نجحت التجربة الأمريكية: قام المقتطف "المترجم" بتوجيه المقص الجزيئي Cas9 بدقة إلى مقطع الحمض النووي المتحور وفصله. الآن أصبحت آليات الإصلاح الخاصة بالخلية قادرة على استعادة الجين.
حتى أن النجاح أذهل العلماء أنفسهم: اختفت الطفرة المسببة للأمراض في 42 جنينًا - بمعدل نجاح 72 بالمائة.
يقول جون وو ، أحد مؤلفي الدراسة: "في مزارع الخلايا ، لم تعمل تقنية CRISPR / Cas9 بشكل جيد مع الأجنة الحية لفترة طويلة". يعتقد الباحثون أن السبب في ذلك هو آلات إصلاح الحمض النووي التي تعمل بشكل جيد في المراحل الجنينية المبكرة.
كما أن تجربة سابقة قام بها علماء صينيون في أبريل 2015 كانت أسوأ بكثير من تجربة الباحثين الأمريكيين. على عكس ميتاليبوف وفريقه ، أضاف الصينيون مقص الجينات فقط إلى البويضة الملقحة مع مترجمهم - وليس في وقت الإخصاب.
مقص خارج السيطرة
وكان على الباحثين الصينيين التعامل مع مشكلة أخرى لم تواجهها تجربة ميتاليبوف: ما يسمى بالطفرات غير المستهدفة. تعتبر أكبر خطر عند استخدام CRISPR / Cas9.
يعني عدم الهدف أن المقص الجيني يقطع أيضًا في أماكن أخرى غير التي تريدها. ولا يمكن إعادة تجميع كل شيء بشكل صحيح من خلال إصلاحات الخلية الخاصة. ثم تظهر طفرات جديدة يمكن أن تؤدي إلى الإصابة بالسرطان ، على سبيل المثال.
"نحن نقود سيارة ما زلنا نبنيها".
من خلال محاولتهم ، أعاد ميتاليبوف وزملاؤه إشعال الجدل الأخلاقي حول ما إذا كان يُسمح للبشر بالتلاعب بالأجنة. في ألمانيا حتى الآن يُسمح فقط بما يُسمى بتشخيص ما قبل الزرع. يتضمن ذلك فحص المادة الوراثية للأجنة بعد التلقيح الصناعي خارج الرحم واستخدام الأجنة السليمة فقط - أي تلك التي لا تحمل مرضًا وراثيًا خطيرًا مثل HCM. ولا يجوز استخدام الطريقة إلا إذا كان هناك خطر من الإصابة بمرض وراثي خطير.
يمكن لتقنية CRISPR / Cas9 أيضًا أن تشفي الأجنة التي سيتم اختيارها أثناء تشخيص ما قبل الزرع. نظريا. لأنه يبقى أن نرى ما إذا كان من الأفضل حقًا. لا يمكن تقييم المخاطر المرتبطة بالعلاج بالمقص الجيني بشكل نهائي - يتفق العلماء على ذلك. قال جاكوب كورن ، مدير مبادرة الجينوم في جامعة كاليفورنيا في بيركلي ، عن حالة بحث CRISPR / Cas9: "نحن نقود سيارة ما زلنا نبنيها".
مخاطر غير معروفة
تدعو إحدى عشرة منظمة علمية أمريكية رئيسية إلى "نهج حذر ولكنه ملتزم" في المجلة الأمريكية للوراثة البشرية. حتى تعرف ما إذا كانت الفوائد تفوق المخاطر حقًا. لذلك يعتبر الباحثون أنه من "غير المناسب حاليًا" إدخال جنين معدل وراثيًا من امرأة وإحداث الحمل.
تم تدمير أجنة CRISPR / Cas من تجربة ميتاليبوف بعد بضعة أيام. في هذا الوقت ، يتكون الجنين من كرة خلوية صغيرة مملوءة بسائل ، هي الكيسة الأريمية. لم يعرّف العلماء بعد هذه المرحلة الجنينية بأنها حياة الإنسان. إذا لم تزرع الكيسة الأريمية نفسها في الرحم ، يتم إنشاء الخلايا الجذعية الجنينية "فقط" منها في المختبر.
يمكن بالطبع مناقشة مسألة متى تبدأ الحياة. في ألمانيا ، على سبيل المثال ، لا يجوز تجميد الأجنة إلا في مرحلة ما يسمى بالمرحلة النووية ولغرض الإخصاب الصناعي وتدميرها في مرحلة ما. معهم ، لم يتم دمج نواة خلية البويضة تمامًا مع السائل المنوي. يدعو العديد من الباحثين إلى استخدام مثل هذه الهياكل لأهداف بحثية عالية المستوى.
أطفال مصمم؟
ولكن إلى أي مدى يمكنك أن تذهب في البحث الجيني والعلاج؟ لدى مكتشف CRISPR / Cas9 Doudna مخاوف ويقول: "غالبًا ما سألت نفسي عما سيفعله الباحثون بهذه التكنولوجيا ، وأنا مسؤول عن وجودها جزئيًا." ، ولكن أيضًا تحديد لون الشعر ولون العين والذكاء والشخصية - إذا لم يتم منع مثل هذه التجربة بموجب القانون مسبقًا. لقد حان الوقت لتحديد المخاطر التي يُسمح للباحثين بمواجهتها عند تعديل الأجنة وراثيًا وأي التلاعب يجب حظره من حيث المبدأ.
* تم تغيير الاسم من قبل المحرر.
كذا: الحيض مجلة العناية بالبشرة










-mit-tattoos-dem-schicksal-trotzen.jpg)