اللقاحات: تصنيعها واعتمادها
درست Martina Feichter علم الأحياء من خلال صيدلية متخصصة في إنسبروك وانغمست أيضًا في عالم النباتات الطبية. من هناك لم يكن بعيدًا عن الموضوعات الطبية الأخرى التي ما زالت تأسرها حتى يومنا هذا. تدربت كصحفية في أكاديمية أكسل سبرينغر في هامبورغ وتعمل في منذ عام 2007 - في البداية كمحرر ومنذ عام 2012 ككاتبة مستقلة.
المزيد عن خبراء يتم فحص جميع محتويات بواسطة الصحفيين الطبيين.
تُستخدم اللقاحات لحمايتك وحماية الآخرين: يمكنها أن تمنعك من الإصابة بالمرض ومن احتمال إصابة الآخرين بالعدوى. اقرأ هنا ما هي أنواع اللقاحات الموجودة وكيف يتم صنعها وكيف يتعين عليها إثبات فعاليتها وسلامتها!

ما هي اللقاحات؟
اللقاحات عقاقير من المفترض أن تجعل الجسم محصنًا ضد بعض مسببات الأمراض. لذلك يمكنك الحماية من العدوى ، ولهذا يتحدث المرء عن التطعيم.
يصنف الخبراء اللقاحات وفقًا لمعايير مختلفة. يتم التمييز بين اللقاحات الحية واللقاحات الميتة وفقًا لجدوى أو قدرة مسببات الأمراض الموجودة على التكاثر. يمكنك قراءة المزيد حول هذا الموضوع في مقال "اللقاحات الحية والميتة".
تحتوي اللقاحات المؤتلفة على عنصر معدّل وراثيًا ومكوّنًا نموذجيًا بشكل خاص لمسببات الأمراض (مستضد الوحدة الفرعية). إذا كان ما يسمى بالفيروسات النواقل (الحية ، ولكن ليست الفيروسات المسببة للأمراض) تحمل هذا المستضد النموذجي على سطحها ، فإن بعض الخبراء يتحدثون عن لقاح حي مأشوب.
تقدم اللقاحات الجينية فقط المخطط الجيني لمستضدات العامل الممرض في الجسم. باستخدام هذه التعليمات ، يجب على الجسم بعد ذلك إنتاج المستضدات الأجنبية نفسها ، والتي تؤدي في النهاية إلى استجابة مناعية. تشمل هذه الأنواع من اللقاحات لقاحات DNA و mRNA ، بالإضافة إلى لقاحات ناقلات. تمت الموافقة عليها لأول مرة ضد Covid-19 (لقاح فيروس كورونا).
كيف تصنع اللقاحات؟
عادة ، يتم زراعة مسببات الأمراض ذات الصلة على نطاق واسع لإنتاج اللقاحات. ثم يتم معالجتها ، كليًا أو جزئيًا ، في لقاح. هناك أيضًا بعض اللقاحات التي تحتوي على مستضدات لممرض تم إنتاجه باستخدام الهندسة الوراثية أو مخططها.
طريقة التطوير
يتم تطوير اللقاح بشكل عام في عدة خطوات:
- تحليل العوامل الممرضة وتحديد المستضد المناسب الذي يثير استجابة مناعية
- التحقيق وتعريف "تصميم" اللقاح (لقاح ميت أو لقاح حي؟ مسببات الأمراض الكاملة أو مكوناتها؟ استخدام الهندسة الوراثية؟)
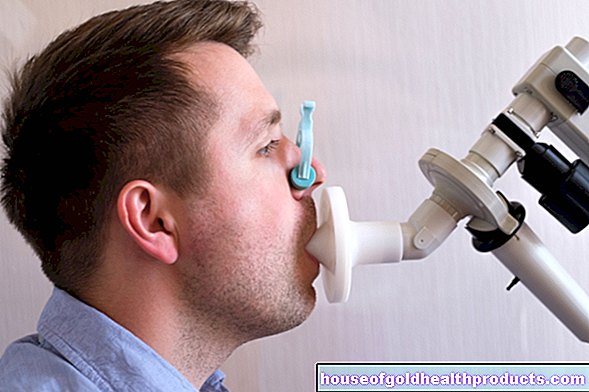
- اختبارات مكثفة في المختبر ، على سبيل المثال على الحيوانات ، ثم على البشر ؛ كما كان الحال قبل الموافقة على الأدوية ، تتم هذه على ثلاث مراحل. يختبر العلماء الجرعة والتحمل والاستجابة المناعية على المزيد والمزيد من المتطوعين.
- إجراءات الموافقة في هيئة التطعيمات
يجب أن يؤدي التطعيم دائمًا إلى استجابة مناعية مستقرة ، والتي تنتج بشكل مثالي حماية مناعية أفضل وأطول أمداً من العدوى الفعلية. ومع ذلك ، يجب ألا يؤدي هذا إلى رد فعل دفاعي مفرط من شأنه في النهاية أن يضر أكثر مما ينفع. في تطوير اللقاح ، من المهم أيضًا تحمل اللقاح.
صنع لقاح
يتم إنتاج اللقاح نفسه بالطريقة التالية:
- زراعة مسببات الأمراض التي يعمل اللقاح ضدها ، أو الهندسة الوراثية للمستضدات المرغوبة أو مخطط المستضد المناسب
- "حصاد" المستضدات ، على سبيل المثال الفيروسات من مزارع الخلايا أو المستضدات من خلايا الخميرة ، أو المخطط الجيني والمعالجة اللاحقة
- إضافة مكونات أخرى ، على سبيل المثال لتقوية تأثير التطعيم (المواد المساعدة) ، ودمج المكونات في اللقاحات المركبة
- التعبئة والتغليف
زراعة مسببات الأمراض
يمكن زراعة مسببات الأمراض اللازمة لإنتاج لقاحات ضد الأمراض المعدية البكتيرية (مثل المكورات السحائية ، وبكتيريا التيفوئيد) مباشرة في وسط المغذيات. توفر هذه الوسائط الثقافية لمسببات الأمراض كل ما يحتاجونه للبقاء والتكاثر. ثم يتم معالجتها في لقاح في عدة خطوات.
يعد إنتاج لقاحات ضد الأمراض المعدية الفيروسية (مثل الأنفلونزا والحصبة والنكاف والحصبة الألمانية) أكثر تعقيدًا لأن الفيروسات يمكن أن تتكاثر فقط في الخلايا الحية. لزراعة الكمية الهائلة من مسببات الأمراض اللازمة لإنتاج اللقاح ، يحتاج المرء إلى خلايا مضيفة حية:
بيض الدجاج
يُستخدم بيض الدجاج تقليديًا لزراعة الفيروسات: يتم حقن بعض الفيروسات ("فيروسات البذور") في بيضة دجاج مخصبة ، ثم يتم تحضينها في حاضنة. خلال هذا الوقت ، تتكاثر مسببات الأمراض في الداخل. بعد بضعة أيام ، يتم عزلهم في عمليات معقدة ومعالجتهم في لقاح.
بيض الدجاج المستخدم ليس بيض عادي صالح للاستهلاك ومتوفر في محلات البقالة. وبدلاً من ذلك ، يأتي بيض صنع اللقاحات الفيروسية من الدجاج الذي يتم الاحتفاظ به في مزارع خاصة تحت ظروف خاضعة للرقابة. يجب أن تفي بمعايير الجودة العالية وأن تكون خالية تمامًا من مسببات الأمراض الأخرى ("تربية الدجاج المعقمة").
تم إثبات تصنيع اللقاحات القائمة على البيض ، ولكنه أيضًا يستغرق وقتًا طويلاً: قد يستغرق إكمال عملية التصنيع من ستة إلى اثني عشر شهرًا. بالإضافة إلى ذلك ، هناك حاجة إلى كميات ضخمة من البيض الخاص لإنتاج اللقاح - فقط للقاح الإنفلونزا ، والذي يتم تصنيعه بشكل حصري تقريبًا بهذه الطريقة. في جميع أنحاء العالم ، هناك حاجة إلى حوالي نصف مليار بيضة دجاج لهذا كل عام. لأن جرعة واحدة من لقاح الإنفلونزا تحتاج بيضة أو بيضتين.
مزارع الخلايا
يمكن الحصول على فيروسات لقاح بسرعة وكفاءة أكبر من الخلايا الحيوانية أو مزارع الأنسجة. يأتون من القرود والهامستر والكلاب أو الأجنة البشرية. هناك أيضًا سلالات خلوية تم تخليدها وراثيًا في المختبر وبالتالي يمكن استخدامها على المدى الطويل لزراعة فيروسات اللقاح.
من أجل الإنتاج المؤتمت بالكامل على نطاق واسع ، طور الباحثون تقنيات لزراعة خطوط الخلايا في حاويات كبيرة (مخمرات أو مفاعلات حيوية) - تطفو في وسط سائل تُضاف إليه جميع المواد باستمرار والتي تحتاجها الخلايا للبقاء على قيد الحياة والانقسام.
يستخدم الموظفون المجسات لمراقبة إمدادات المغذيات ، وإذا لزم الأمر ، قم بتعديلها مع العدد المتزايد من الخلايا. تقوم المضخات الخاصة باستمرار بترشيح نفايات الخلايا واستخدام محلول المغذيات. بمجرد الوصول إلى كثافة خلية معينة ، تتم إضافة الفيروسات المطلوبة للقاح. تصيب الخلايا ، مما يسمح لها بالتكاثر بأعداد كبيرة.
إن نمو الفيروسات في مزارع الخلايا بدلاً من بيض الدجاج له ميزة أخرى بالإضافة إلى وقت الإنتاج الأقصر: اللقاحات المقابلة مضمونة لتكون خالية من بروتين الدجاج وبالتالي فهي مناسبة أيضًا للأشخاص الذين لديهم حساسية من بروتين الدجاج. على سبيل المثال ، هناك لقاحات الأنفلونزا القائمة على زراعة الخلايا.
الهندسة الوراثية
ليس من الضروري دائمًا مضاعفة مسببات الأمراض حتى تتمكن من إنتاج لقاح منها. بمجرد أن يقوم العلماء بفك رموز المخطط الجيني لمولدات المضادات الخاصة بهم ، يمكن إعادة إنشاء هذا أو أجزاء منه في المختبر باستخدام طرق الهندسة الوراثية. يتم تهريب المخططات المنتجة صناعيًا إلى البكتيريا أو خلايا الخميرة ، على سبيل المثال ، والتي تنتج بعد ذلك المستضدات الغريبة. تتوفر هذه "اللقاحات المؤتلفة" ضد الهربس النطاقي (القوباء المنطقية) والتهاب الكبد B وفيروس الورم الحليمي البشري (HPV).
أو يمكن للباحثين استخدامه للحصول على مخطط للمستضد المطلوب ، والذي من المفترض أن يقوم بتشغيل جهاز المناعة في جسم الإنسان بعد التطعيم. إذا لزم الأمر ، تتم معالجة خطط البناء هذه (على سبيل المثال ، يتم ترجمة الحمض النووي الوراثي الذي تم الحصول عليه إلى RNA الرسول) و "تعبئتها". يتم استخدام قطرات صغيرة من الدهون لهذا الغرض ، أو يتم توجيه مقتطفات DNA / RNA إلى فيروسات حاملة غير ضارة (نواقل). هذه "العبوة" مهمة لأن المخططات الجينية حساسة للغاية ويتم تفكيكها بسرعة.
القبول والأمن
تخضع الموافقة على لقاح جديد لرقابة صارمة. يجب على الشركة المصنعة تقديم العديد من المستندات حول سلامة وفعالية الدواء الجديد إلى السلطة المختصة (انظر أدناه: سلطات التطعيم). وتشمل هذه في المقام الأول:
- بيانات عن جودة اللقاح فيما يتعلق بعملية التصنيع وما يرتبط بها من إجراءات ضمان الجودة والمراقبة
- بيانات عن الاختبارات قبل السريرية للقاح على الحيوانات
- بيانات عن الفعالية والآثار الجانبية للقاح كما وجدت في الدراسات السريرية البشرية
توجد إرشادات دقيقة لضمان جودة عمليات الإنتاج والبيئة الخاصة باللقاحات والمستحضرات الصيدلانية الأخرى. تتضمن "ممارسات التصنيع الجيدة" (GMP) توثيقًا لجميع خطوات العمل بالإضافة إلى مراجعة دورية للمختبرات والأجهزة والموردين والمواد الخام.
تقوم سلطة الترخيص بمراجعة وتقييم جميع الوثائق المقدمة ثم تقرر ما إذا كان اللقاح الجديد سيوافق أم لا. يمكنك معرفة المزيد عن إجراءات الموافقة على الأدوية في مقالتنا "الموافقة على الأدوية".
مراقبة ما بعد الموافقة
حتى بعد الموافقة عليه ، تراقب السلطات اللقاح. في ألمانيا ، معهد Paul Ehrlich (PEI ، انظر أدناه) هو المسؤول عن ذلك. يستعرض جودة وفعالية وسلامة كل دفعة من اللقاحات. فقط إذا لم يكن لدى الخبراء ما يشكو منه ، يتم إصدار الدفعة للسوق.
بالإضافة إلى ذلك ، فإن الأطباء ملزمون بالإبلاغ عن أي آثار جانبية غير متوقعة للتطعيم إلى جزيرة الأمير إدوارد. من الممكن ألا يتم تسجيل آثار جانبية نادرة جدًا أو آثار طويلة الأمد للتطعيم في دراسات الموافقة السريرية. على أساس الآثار الجانبية المبلغ عنها ، يمكن أن تطلب PEI ، إذا لزم الأمر ، تحذيرات إضافية من الشركة المصنعة في نشرة العبوة ، أو تطلب سحب مجموعة لقاح فردية أو إلغاء الموافقة على اللقاح تمامًا.
سلطات التطعيم
يجب أن يتغلب اللقاح الجديد على العديد من العقبات ويلبي لوائح السلامة الصارمة قبل أن يتمكن الأطباء من إدارة هؤلاء الأشخاص. لهذا السبب ، تم إنشاء هيئة رقابة في ألمانيا منذ أكثر من 100 عام لرعاية اختبار اللقاحات والموافقة عليها: معهد Paul Ehrlich (PEI) في لانغن بالقرب من فرانكفورت أم ماين.
وهي تعمل بشكل وثيق مع وكالة الأدوية الأوروبية (EMA) ومقرها أمستردام. في هذا البلد ، تهتم اللجنة الدائمة للتلقيح (STIKO) في معهد روبرت كوخ بتقييم المخاطر والفوائد لتوصيات التطعيم والتطعيم.
معهد بول إيرليخ (PEI)
تم تخصيص معهد Paul Ehrlich لوزارة الصحة الفيدرالية. يشرف على جميع اللقاحات والأدوية الطبية الحيوية (مثل الأجسام المضادة العلاجية ، ومستحضرات الدم والأنسجة ، وأدوية العلاج الجيني).
تقع المهام التالية ضمن نطاق مسؤولية جزيرة الأمير إدوارد:
- الموافقة على التجارب السريرية للقاحات
- معالجة طلبات الموافقة على اللقاحات الجديدة وكذلك طلبات المتابعة والتغييرات المطلوبة على الموافقات الحالية
- اختبار الدولة والموافقة على دفعات اللقاح
- تقييم سلامة الدواء (جمع وتقييم الآثار الجانبية التي أبلغ عنها الأطباء)
- البحث في مجالات الحساسية ، والبكتيريا ، والتكنولوجيا الحيوية ، والمناعة ، وأمراض الدم ، وطب نقل الدم ، والطب البيطري ، وعلم الفيروسات
- تقديم المشورة للهيئات الوطنية والأوروبية والدولية بشأن تقييم المخاطر وتطوير المبادئ التوجيهية
وكالة الأدوية الأوروبية (EMA)
تقوم وكالة الأدوية الأوروبية (الوكالة الأوروبية للأدوية) بمهام مماثلة على المستوى الأوروبي لمعهد بول إيرليش في ألمانيا. تتمثل إحدى مهامهم الرئيسية في الموافقة على المنتجات الطبية ومراقبتها داخل الاتحاد الأوروبي - ليس فقط اللقاحات والمنتجات الطبية الطبية الحيوية ، ولكن أيضًا المنتجات الطبية الأخرى. بالإضافة إلى ذلك ، مثل PEI ، يجمع EMA تقارير عن الآثار الجانبية التي تحدث. بالإضافة إلى ذلك ، يمكنها - إذا لزم الأمر - سحب الموافقة على دواء أو طلب تحسينات من قبل الشركة المصنعة.
يعمل EMA بشكل وثيق مع السلطات التنظيمية الوطنية في دول الاتحاد الأوروبي - وكذلك مع المديرية العامة للصحة في مفوضية الاتحاد الأوروبي والوكالات الشقيقة مثل المركز الأوروبي للوقاية من الأمراض ومكافحتها (ECDC).
اللجنة الدائمة للتطعيم (STIKO)
يعتمد موعد وكيفية إعطاء اللقاحات إلى حد كبير على توصيات التطعيم الصادرة عن لجنة التطعيم الدائمة (STIKO) في معهد روبرت كوخ. على سبيل المثال ، تنشر STIKO تقويمات التطعيم لجميع الفئات العمرية. لا توصي باللقاحات الفردية ، ولكنها تقيم بشكل أساسي الأمراض التي يمكن الوقاية من التطعيم لها - ولمن.
توصيات STIKO ليست ملزمة قانونًا في البداية. إذا وافقت اللجنة الفيدرالية المشتركة (G-BA) على التقييم ، يتم تضمين التطعيم الموصى به في كتالوج المزايا الإلزامية للتأمين الصحي القانوني.
مثل معهد Paul Ehrlich ووكالة الأدوية الأوروبية ، تشارك لجنة التطعيم الدائمة أيضًا في تسجيل الآثار الجانبية غير المتوقعة - حتى ولو بشكل غير مباشر. يطور STIKO معايير للتمييز بين تفاعلات التطعيم الشائعة (مثل احمرار الجلد) من الأحداث الخطيرة. علاوة على ذلك ، تقدم STIKO نصائح حول كيفية التعامل مع اختناقات توصيل اللقاح ، أي نقص اللقاحات.
اللقاحات: التطورات الجديدة
تمت الموافقة على اللقاحات حاليًا ضد حوالي 30 مرضًا. في بعض الحالات ، تعمل شركات الأدوية على تطوير لقاحات أفضل ضد بعض هذه الأمراض. هناك لقاحات جديدة ضد المكورات الرئوية تعمل على الحماية من أنواع فرعية من الممرض البكتيري أكثر من لقاحات المكورات الرئوية المتوفرة سابقًا.
بالإضافة إلى ذلك ، يتم إجراء الأبحاث على لقاحات جديدة تمامًا - أي لقاحات ضد الأمراض التي لم يتم تطعيمها بعد ، مثل الإيدز. يعمل الباحثون أيضًا على تطوير لقاح ضد فيروسات النوروفيروس. هذه العوامل الممرضة هي مسببات متكررة لالتهابات الجهاز الهضمي مع الإسهال والقيء في جميع أنحاء العالم.
يبحث العلماء أيضًا بشكل مكثف عن العمليات الجديدة التي تتيح إنتاج لقاح أسرع وأكثر كفاءة. ينصب التركيز هنا على اللقاحات الجينية المذكورة أعلاه. كجزء من وباء كورونا ، وافقت السلطات على لقاحات هذا الجيل الجديد لأول مرة (التطعيم ضد فيروس كورونا).
أخيرًا وليس آخرًا ، تعتبر اللقاحات العلاجية أيضًا موضوعًا للبحث. الهدف ليس الوقاية من المرض ، ولكن علاجه - على سبيل المثال ، سرطان عنق الرحم الناجم عن فيروس الورم الحليمي البشري. يريد العلماء أيضًا طرح لقاحات علاجية في الأسواق. ضد فيروس نقص المناعة البشرية ، على سبيل المثال ، من المفترض أن "يدفع" الجهاز المناعي للمريض حتى يتمكن من السيطرة على الفيروسات.
كذا: السن يأس نايم نصيحة كتاب
-bei-kindern.jpg)